Ⅰ. 서 론
Benzyl alcohol(BzOH)은 식품에는 착향제(0.01% 농도)로, 화장품에서는 (5∼10% 농도), 그리고 제약 산업에서 착향제와 방부제로서 사용되고 있는 물질로 알려져 있으며, 안전성에 대한 연구가 진행된 물질로 알려져 있다(1, 2). 그러나, 몇몇 BzOH의 독성 및 알러지 문제가 보고되고 있다(3-7). 본 연구팀에서는 이러한 BzOH의 문제를 해결하기 위한 방법으로 benzyl alcohol galactoside(BzO-gal)를 합성하여, 이를 BzOH의 대체 후보물질로 사용하려는 연구를 수행하였다(8, 9). 이는 그동안 본 연구팀의 chlorphenesin(CPN)(10, 11), phenoxyethanol(PE)(12, 13), 1,2-hexanediol(HD)(14-17), 그리고 1,2-octanediol(OD)(18, 19)의 galactoside 유도체(CPN-gal, PE-gal, HD-gal, OD-gal) 합성과 그들의 특성 연구에 기반을 두고 이루어진 것이다. 지금까지의 연구 결과를 종합해 보면, CPN-gal, PE-gal, HD-gal, 그리고 OD-gal과 같은 galactoside 유도체의 특징은 galactose 한 분자가 결합하여 합성된 galactoside 유도체 분자 모두가 CPN, PE, HD, 그리고 OD에 비하여, 인간 피부세포(HACAT cell)에 대한 독성이 현저하게 감소되었다는 것이었다(11, 13, 17, 19). 이러한 결과는 이들 galactoside 유도체가 인간 세포에 대한 독성을 감소시킬 수 있는 물질로서 개발될 가능성을 보여주는 것이라 하겠으며, 본 연구에서도 이를 기반으로 BzOH의 문제를 해결할 수 있는 전략으로 BzO-gal의 합성과 이용에 관심을 가지고 연구를 수행하게 되었다.
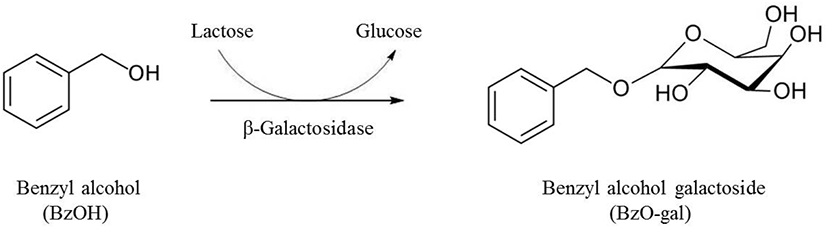
이미 위의 선행연구를 근거로 하여 대장균(Escheichia coli, E. coli)의 β-galactosidase(β-gal)를 이용하여 BzOH로부터 transgalactosylation 반응(Figure 1)으로 BzOH에 galactose 한 분자가 결합한 BzO-gal을 합성하였고(8), 합성반응에 대한 기초연구도 추가로 수행하였다(9). 이러한 transgalactosylation 반응은 30%에서 35%의 고농도의 lactose가 존재하는 반응 환경에서 일어나는 역가수분해반응(reverse hydrolysis)으로 설명할 수 있다. 다시 말하면, β-gal이 lactose를 가수분해하는 반응보다 BzOH에 galactose를 붙여서 BzO-gal을 합성하는 반응에 더 선호도를 가지게 된다. 이때, galactose는 일부 lactose의 가수분해물에서 공급되게 된다(Figure 1).
본 연구에서는 BzOH보다 BzO-gal이 상대적으로 독성이 적을 것으로 추론하고, 이를 BzOH의 대체물질로 사용하기 위한 기초연구를 수행하였다. 특히, 본 연구에서는 산업적 실용화를 위한 기초 단계 연구로서 합성된 BzO-gal이 항균력을 가지고 있는지에 대한 조사를 위하여 실제 식품에 적용하여 BzO-gal의 항균력을 관찰하였다. 이를 위하여 충북 진천의 ㈜제이엔제이푸드(J&J Food Co.)에서 생산되는 화이트소스(white sauce)에서 E. coli ATCC 25922에 대한 항균력을 BzOH와 비교하여 조사하였다. 하지만, 반응액으로부터 순수하게 정제된 BzO-gal의 사용은 정제 비용 등의 추가 비용이 필요하여 산업적 실용화 가능성을 낮게 하기 때문에 BzO-gal이 들어있는 반응액을 항균력 조사에 사용하였다. 반응액에는 합성된 BzO-gal과 BzOH가 거의 같은 비율로 존재하기 때문에 반응액의 항균력 조사 결과를 바탕으로 BzO-gal의 항균력을 추론하려고 하였다.
아직까지는 BzOH가 식품첨가물 중 방부제로 사용되고 있지 않고, 식품공전에도 BzOH가 방부제가 아닌 조향제로 등록이 되어 있다(20). 그러나 본 연구에서는 앞으로 식품, 화장품 및 제약 분야 등 다양한 산업 분야에서 사용될 가능성을 염두에 두고, 그 대안으로서의 BzO-gal에 대한 항균력을 조사하였다.
Ⅱ. 재료 및 방법
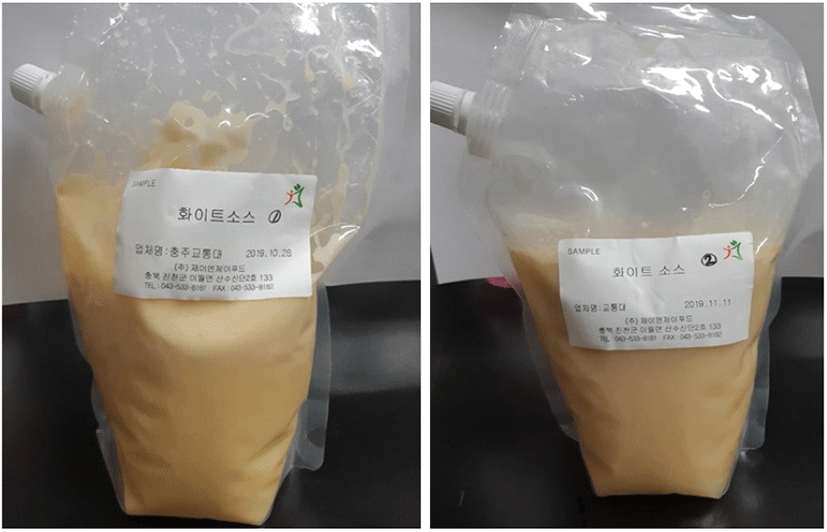
Benzyl alcohol은 Sigma-Aldrich(St. Louis, MO, USA)에서 구입하여 사용하였고, TLC(thin-layer chromatography) plate는 Macherey–Nagel(Düren, Germany)의 DC-Fertigplatten SIL G-25 UV254를 사용하였다. 기타 본 연구에 사용한 시약들은 reagent-grade를 사용하였다. 그리고 본 연구에 사용한 화이트소스는 충북 진천의 ㈜제이엔제이푸드(J&J Food Co.)에서 제공하였고, 마요네즈가 첨가된 것은 화이트소스 1, 마요네즈가 첨가되지 않은 것은 화이트소스 2로 명명한 후 사용하였다(Figure 2). 그리고, 그 조성은 Table 1에 표시하였다.
β-Gal을 생산하는 재조합 대장균, 그리고 발현과 관련된 프로모터 시스템과 재조합 대장균의 배양하여 β-gal을 생산하는 방법 등에 대하여 선행연구에서 자세히 기술하였다(21).
50 mM phosphate buffer(pH 7.5)를 이용하여 50 mL conical tube에서 350 g/L lactose, 0.75 U/mL β-gal, 2%(w/v) BzOH를 녹인 후, shaking incubator(40℃, 100 rpm)에서 48시간 동안 반응시켜 BzO-gal을 합성하였다. 합성반응 후, 반응물을 화이트소스에 사용하는 항균제로 사용하였다.
Deep freezer에 보관된 E. coli ATCC 25922의 한 vial(1.0 mL)를 멸균된 LB 액체 배지(tryptone; 10 g/L, yeast extract; 5 g/L, NaCl; 10 g/L)에 접종하여 12시간이 지난 후, 새 LB 액체 배지에 접종하여 배양한다. 그리고, 12시간 정도 배양한 후 OD 값(at 600 nm)이 2.0이 되게 배양한다.
Table 2와 같이 세 개의 실험 set(Experiment #1, #2, #3)을 구상하고, 각 실험 set마다 세 개의 용액(Solution #1, #2, #3)을 준비하였다. 각 실험 set의 Solution #1은 반응액(10 mL)과 화이트소스(10 mL)의 혼합액, Solution #2는 control로서 BzOH(10 mL)와 화이트소스(10 mL)의 혼합액, Solution #3은 멸균 증류수(10 mL)와 화이트소스(10 mL)의 혼합액으로 만들어져 멸균하여 준비하였다. Table 2에 나오는 약어는 Table 3에 설명하였다.
항균력 조사를 위한 실험을 위하여 위에서 배양한 E. coli ATCC 25922의 배양액 700 μL를 Table 2의 Experiment #1, #2, #3의 Solution #1, #2, #3에 각각 접종한다. 그리고, shaking incubator(37℃, 200 rpm)에서 12시간 배양하고, 이 배양액을 사용하여 LB agar plate에 백금이로 streaking한다. 약 18시간이 지난 후, LB agar plate에 E. coli ATCC 25922가 colony를 형성하고 자라는지를 확인하여, E. coli ATCC 25922에 대한 항균력이 있는지를 관찰하였다.
20 × 10 cm TLC plate에 1.0 μL 시료를 loading하고 이동상(acetonitrile : water = 85 : 15(v/v))을 이용하여 15분 전개하였다. 그리고 staining solution(1.5 g KMnO4, 10 g K2CO3, 1.25 mL 10% NaOH in 200 mL water)을 TLC plate에 뿌린 후, 80℃ oven에서 15분간 말려서 밴드를 확인하였다. 합성반응이 끝난 후, 반응액 중의 BzOH와 BzO-gal의 함량 분석을 위하여, 합성반응액의 TLC 분석 plate를 스캔하여 BzOH와 BzO-gal 이미지를 얻고, 그 이미지를 AlphaEase FC software (Alpha Innotech, San Leonardo, CA, USA)를 이용하여 정량적으로 분석하였다.
Ⅲ. 결과 및 고찰
BzO-gal의 E. coli에 대한 항균력 조사하기 위하여, 먼저 E. coli β-gal을 이용하여 2% BzOH를 사용하여 BzO-gal을 합성하였다(Figure 3). 그리고, 반응액 중의 BzO-gal과 BzOH의 함량 비율을 TLC data의 BzOH와 BzO-gal 이미지를 이용하여 정량적으로 분석하였다. 그 결과, Figure 3에서 같이 BzOH와 BzO-gal의 함량 비율은 각각 49.2%와 50.8%로 확인되었다. 반응이 종료된 후, 반응액 중에는 약 1:1의 비율로 BzOH외 BzO-gal이 존재한다는 것을 확인할 수 있었다. 그래서, 반응액 중의 BzOH와 BzO-gal의 농도를 약 1% BzOH와 약 1% BzO-gal로 추정하였다. 즉, BzO-gal 합성 반응액 중에는 BzOH와 BzO-gal이 각각 1%씩 들어있음을 확인하였다. E. coli에 대한 항균력 조사에 이 반응액을 사용하였다. 또한, 필요한 경우에는 이 반응액을 2배 농축하여 사용하였다. 즉, 약 2% BzOH와 약 2% BzO-gal이 들어있는 농축된 반응액이 항균력 조사에 사용되었다.

BzOH의 E. coli에 대한 MIC 값(minimum inhibitory concentration)은 0.05∼0.1%로 보고되고 있으나(22), 식품에서는 착향제로 0.01%, 화장품에서는 5∼10% 정도에서 사용되고 있는 것으로 보고되고 있다(2). 그러나, 본 연구에서는 방부제로서의 BzO-gal의 항균력을 조사하기 위한 기초적인 첫 단계로서 약 1% BzOH와 1% BzO-gal이 함유된 반응액을 사용하여 E. coli에 대한 항균력을 조사하여 보기로 하였다(Figure 3). 만약 BzO-gal이 galactosylation으로 항균력을 잃지 않았다면, 이 반응액은 약 2% BzOH와 같은 항균력을 가지고 있을 것으로 추정하고 실험을 진행하였다.
먼저 Figure 4에서와 같이 세 가지 용액(Solutions #1, #2, #3 in Experiment #1, Table 2)에서 배양된 E. coli ATCC 25922를 LB agar plate에 streaking하여 E. coli가 자라는지를 관찰하였다. Agar plate #1과 같이 약 1% BzOH와 1%의 BzO-gal이 함유된 반응액이 들어간 배양액에서 배양된 경우에는 E. coli의 성장이 관찰되었으나, Agar plate #2와 같이 2% BzOH가 함유된 배양액에서 배양된 경우에는 E. coli의 성장이 관찰되지 않았다. 그리고, Agar plate #3와 같이 control로서 DW가 포함된 배양액에서 배양된 경우에서는 E. coli의 성장이 관찰되었다. 이번 실험에 사용한 모든 용액에 white sauce 1이 1/2씩 들어가 있기 때문에 Solutions #1에는 약 0.5% BzOH와 0.5%의 BzO-gal, Solutions #2에서는 1% BzOH가 들어가 있는 조건에서 항균 실험이 진행된 것이라고 할 수 있다. Figure 4의 결과로 봐서는 결국 0.5% BzO-gal에 해당하는 부분이 항균력을 발휘하지 못하여서 Agar plate #1에서 E. coli의 성장이 관찰된 것으로 추론할 수 있었다. 이 결과로 봐서는 BzO-gal이 항균력을 가지고 있지 않은 것으로 판단할 수 있다.

보다 확실한 BzO-gal의 항균력 확인 실험을 위하여 Figure 5와 같은 Experiment #2를 수행하였다. 이 실험에서는 반응액을 2배로 농축하여, 반응액 중의 BzOH와 BzO-gal의 농도를 2배로 높이고, 이를 4% BzOH 용액과 비교하여 항균력을 조사하였다. 그리고, 실험 편의상 white sauce 1의 농도는 1/2 희석하여 실험을 수행하였다. Figure 4와 같이 세 가지 용액(Solutions #1, #2, #3 in Experiment #2, Table 2)에서 배양된 E. coli ATCC 25922의 LB agar plate에 성장을 조사하였다. Agar plate #1과 같이 2배 농축된 반응액(약 2% BzOH와 2%의 BzO-gal 함유)이 들어간 배양액에서 배양된 경우와 Agar plate #2와 같이 4% BzOH가 함유된 배양액에서 배양된 경우 모두 E. coli의 성장이 관찰되지 않았다. 오직 Agar plate #3와 같이 control로서 DW가 포함된 배양액에서 배양된 경우에서만 E. coli의 성장이 관찰되었다. Experiment #1과 마찬가지로 이번 Experiment #2에서도 1/2배 희석된 white sauce 1이 1/2씩 들어가 있기 때문에 Solutions #1에는 약 1% BzOH와 1%의 BzO-gal, Solutions #2에서는 2% BzOH가 들어가 있는 조건에서 항균 실험이 진행되었다. 결론적으로 Figure 5의 Agar plate #1 결과는 1% BzO-gal이 항균력을 발휘하여 나머지 1%의 BzOH와 함께 E. coli의 성장을 저해한다는 것을 말해주고 있다. 다시 말하면, Agar plate #1과 #2에서의 결과는 1% BzO-gal과 1% BzOH로 이루어진 용액이 2% BzOH 용액을 대체하여 E. coli에 대한 항균력을 발휘할 수 있다라는 것을 말해주고 있다.

Experiment #2의 결과를 다시 확인하기 위하여, 배양액에 혼합 사용되는 White sauce 1 대신 White sauce 2를 사용하는 Experiment #3를 수행하였다. White sauce 1의 경우에는 마요네즈가 포함되어 있어서 용액 제조에 불편한 점이 있었기 때문에 마요네즈가 제거된 White sauce 2를 제조하여 Experiment #3에 사용하였다. Experiment #3는 Experiment #2에서 사용한 Whate sauce 1을 White sauce 2로 교체한 것 이외에는 모두 같은 방법으로 수행되었다. 그 결과, Figure 6과 같이 Figure 5에서 같은 결과를 보여주었다.

세 가지 용액(Solutions #1, #2, #3 in Experiment #3, Table 2)에서 배양된 E. coli ATCC 25922의 LB agar plate에 성장을 관찰하였는데, Agar plate #1과 같이 2배 농축된 반응액(약 2% BzOH와 2%의 BzO-gal 함유)이 들어간 배양액에서 배양된 경우와 Agar plate #2와 같이 4% BzOH가 함유된 배양액에서 배양된 경우 모두 E. coli의 성장이 관찰되지 않았다. 그리고, Agar plate #3와 같이 DW가 포함된 배양액에서 배양된 경우에서만 E. coli의 성장이 관찰되었다. Experiment #1 그리고 #2와 같이 이번 Experiment #3에서도 1/2 배 희석된 white sauce 2가 1/2씩 들어가 있기 때문에 Solutions #1에는 약 1% BzOH와 1%의 BzO-gal, Solutions #2에서는 2% BzOH가 들어가 있는 조건에서 항균 실험이 진행되었다. 마찬가지로 Figure 5에서 얻은 결론처럼 Agar plate #1 결과는 1% BzO-gal이 항균력을 발휘하여 나머지 1%의 BzOH와 함께 E. coli의 성장을 저해한다는 것을 말해주고 있고, 이 Agar plate #1과 #2에서의 결과는 1% BzO-gal과 1% BzOH로 이루어진 용액이 2% BzOH 용액을 대체하여 E. coli에 대한 항균력을 발휘할 수 있다라는 것을 의미하고 있다.
본 연구팀의 그동안 수행한 선행 연구 결과를 종합하여 보면, 미생물에 대한 성장 저해력이 있는 항균 물질에 galactose 한 분자를 결합시키면, 항균력이 유지되는 경우도 있지만, 감소되는 경우도 관찰되었다(16, 19). Figure 4에서의 결과를 보면 0.5%의 BzO-gal이 0.5% BzOH의 항균력을 대체하지 못하는 것으로 관찰되었다. 이 결과는 BzO-gal 분자에 galactose 결합함으로 항균력 손실이 일어났다라는 추론을 할 수 있게 한다. 반면, Figure 5와 Figur 6의 결과는 1% BzO-gal이 1% BzOH의 항균력을 완전히 대체할 수 있다는 것을 보여주고 있다. Figure 4의 결과를 해석한다면, 분명히 BzO-gal의 항균력에는 어느 정도 손실이 있었을 것으로 추론된다. 그러나, Figure 5와 Figure 6의 결과에서는 BzO-gal이 BzOH와 같은 항균력을 유지하는 것으로 보여진다. 이를 다시 해석하면, Figure 5와 Figure 6의 결과는 1% BzO-gal이 1% BzOH와 동일한 항균력을 가지고 있지는 않지만, Experiment #2와 Experiment #3 조건에서는 이를 보상하기에 충분한 양의 BzO-gal이 들어가 있을 수 있다는 생각을 할 수 있다. 만약 0.5%에서 1.0% BzO-gal 사이의 농도에서 실험이 이루어졌다면, BzO-gal의 항균력이 나타나기 시작하는 농도를 관찰할 수 있을 것이라고 생각된다. 그리고, 기존에 보고된 BzOH의 MIC 값에 비하여 적어도 10배 큰 값을 본 실험 조건에서 보였다(22). 하지만, 실험 방법과 실험 조건 등이 서로 매우 다르기 때문에 일어난 차이로 추정되며, 본 연구에서와 같이 BzO-gal과 BzOH를 상호 같은 조건에서 비교하는 경우에는 큰 문제가 없을 것으로 생각된다.
비록 좁은 농도 범위에서의 실험이고, Gram negative 세균인 E. coli에 대한 초보적인 항균력 실험 결과이지만, BzO-gal 분자를 보다 안전한 미래의 항균력을 가지고 있는 식품첨가물로서 연구 개발하기 위한 첫걸음으로 의미 있는 결과라고 할 수 있겠다. 앞으로 광범위한 농도에서 다양한 미생물에 대한 항균력 시험과 인체에 대한 안전성 연구들이 뒤를 이어서 필요할 것이라고 생각되며, 이를 위한 추가 실험을 계획하고 있다.