Article
인삼 사포닌 효능 연구에 대한 리뷰
문범희1, 강지성1, 이향렬1,*
Review about Efficacies and Structures of Ginseng Saponines
Beom-Hee Moon1, Ji-Sung Kang1, Hyang-Yeol Lee1,*
1충청북도 증평군 대학로 61 한국교통대학교 식품생명학부 생명공학전공 27909
1Department of Biotechnology, Korea National University of Transportation, Jeungpyeong 27909, Korea
© Copyright 2021 Institute of Biotechnology and Bioindustry. This is an Open-Access article distributed under the terms of the
Creative Commons Attribution Non-Commercial License (http://creativecommons.org/licenses/by-nc/4.0/) which permits
unrestricted non-commercial use, distribution, and reproduction in any
medium, provided the original work is properly cited.
Received: Nov 16, 2021; Revised: Dec 03, 2021; Accepted: Dec 06, 2021
Published Online: Dec 31, 2021
ABSTRACT
Ginseng is widely used for its promising medicinal properties as well as for its possible tonic effect in traditional medicine. These days, many studies focus on finding new ginsenosides and their specific mechanisms of action. To date, more than 150 ginsenosides have been identified and still being discovered today. Major ginsenosides are Rb1, Rb2, Rc, Rd, Re, Rf and Rg1, which are the most abundant ingredients in ginseng. Although there are many reports on the molecular mechanisms and medical applications of those ginsenosides, many concerns still exist for their application in industries. Especially, compound K, which can be mass-produced by bio-conversion, has been shown that there is a selective antibacterial effect against acne-causing bacteria. Ginsenosides such as compound K can be very good materials for the development of cosmetics with new functional properties.
Keywords: Panaxa ginseng; ginsenosides; saponines; traditional medicine
Ⅰ. 서 론
인삼은 천연 제품 중에서 가장 많이 팔리는 제품 중 하나이며, 전통 의학에 자주 사용되어 왔다. 현재 세계적으로 가장 널리 사용되며, 뿌리, 액체 추출물, 음료, 차 등 식품 산업에도 상업적으로 사용된다(1). 인삼의 추출 성분인 사포닌은 진세노사이드라 불리며 약리학적 효능이 있는 생리활성 성분이다. 혈관 형성, 항암, 면역 강화, 당뇨병 등 다양한 치료에 사용된다(2). Ginsenoside는 dammarane 계열의 구성원이며, 다양한 종류의 당이 결합된 4-ring, 스테로이드 유사 구조를 가지고 있다. Ginsenoside는 최소 2개의 또는 3개의 하이드록실 그룹이 있는데, 이는 자유롭거나 단량체, 이량체, 삼량체의 당이 붙는다. 또한, ginsenoside는 protopanaxadiol(PPD)과 protopanaxatriol(PPT)로 크게 구분된다. PPD 그룹의 당 부분은 3-위치에 dammarane-type triterpine이 붙는 반면, PPT 그룹의 당 부분은 6-위치의 dammarane-type triterpine이 붙는다. PPD에는 ginsenoside Rb1, Rc, Rd 등이 존재하고 PPT에는 ginsenoside Rg1, Re, Rf, Rg2, Rh1 등이 존재한다(3, 4). 현재 진세노사이드는 150종류 이상 발견되어 있는데, 그 중 인삼의 90% 이상을 구성하는 주요 진세노사이드는 Rb1, Rb2, Rc, Rd, Re, Rf 및 Rg1이 있으며 인삼의 뿌리에 가장 풍부하다(2). 이러한 주요 진세노사이드로부터 생체변환된 2차 진세노사이드인 Compound K가 있고, 매우 우수한 항암효과를 가지고 있으며, 또한 생체이용률이 높아 중요하게 여겨지고 있다. 본 연구에서는 다양한 인삼 사포닌 성분의 대부분을 구성하고 있는 여러 진세노사이드의 종류들과 효능을 알아보고자 한다(5).
Ⅱ. 인삼 주성분 진세노사이드의 종류와 효능
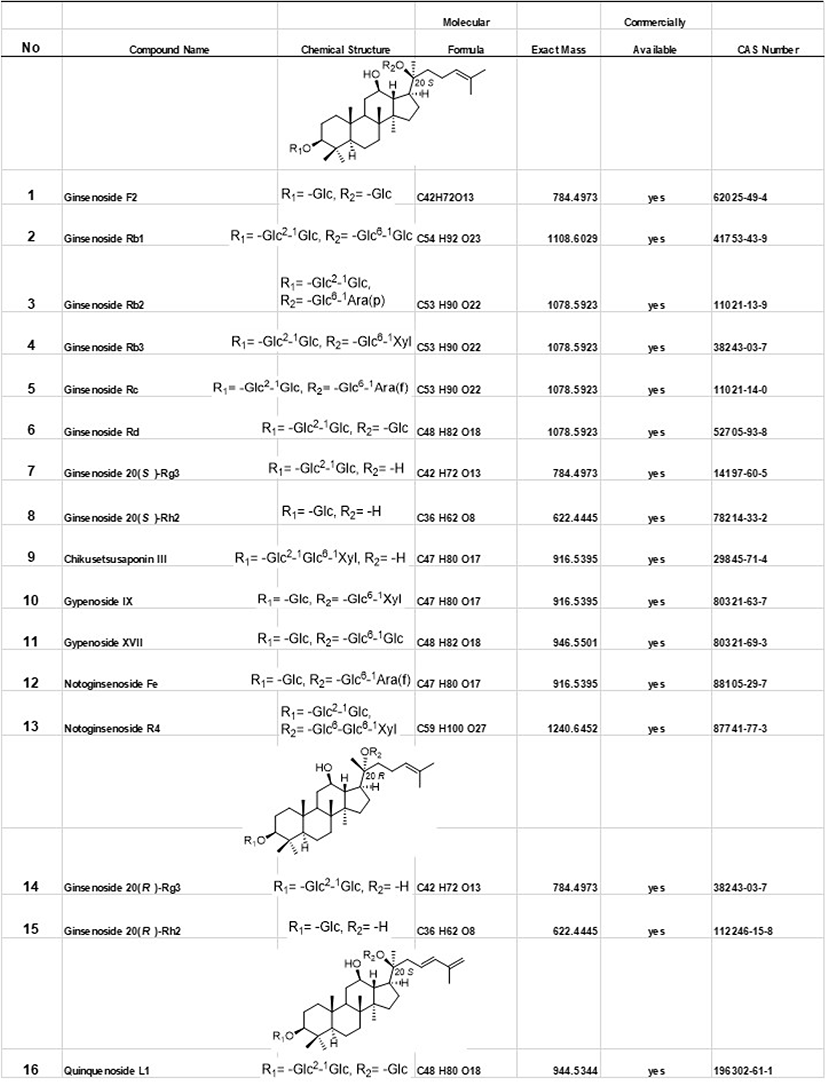
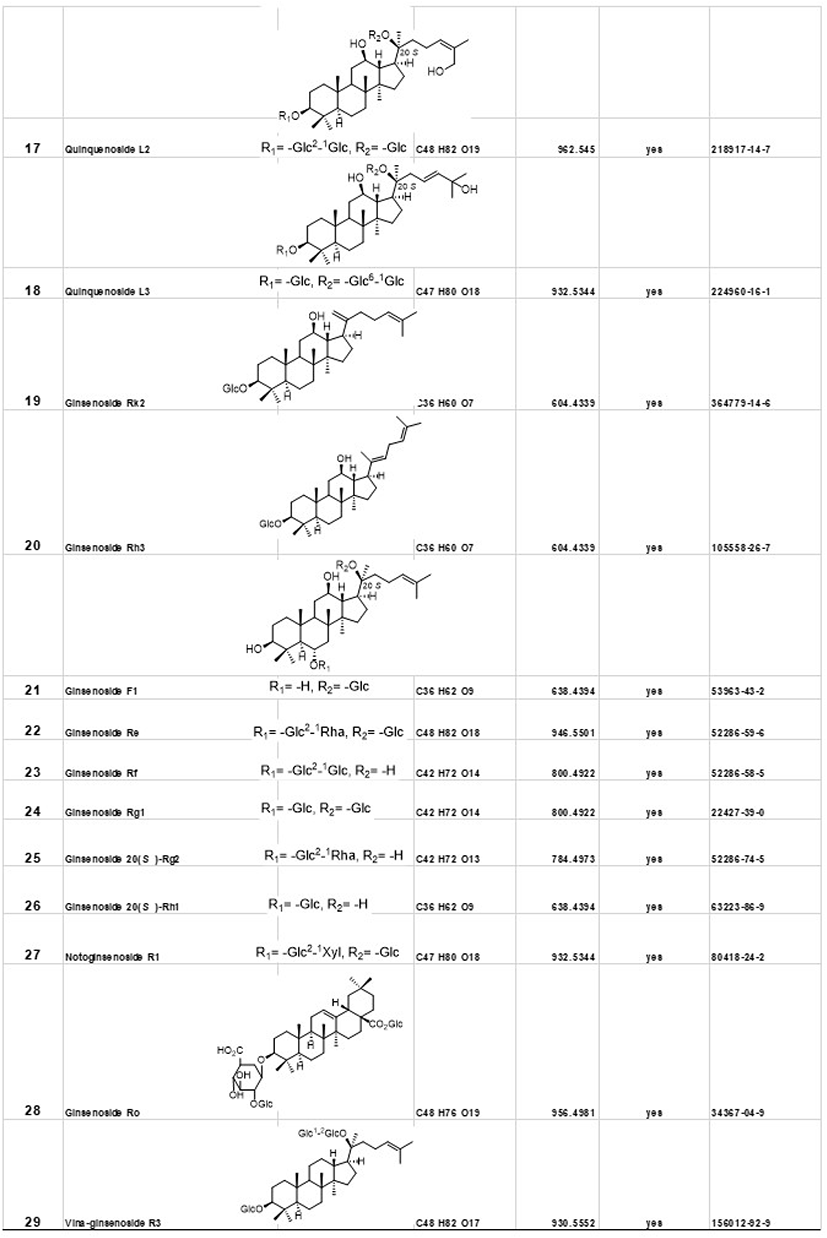
다양한 진세노사이드가 현재에도 발견되고 있으며, 그 구조와 효능에 대해 연구가 되고 있다. 주요한 진세노사이드 중 판매되고 있는 진세노사이드 29종의 화학적 구조 및 분자식, 분자질량을 Figure 1에 나타내었다.
1. 진세노사이드 Rb1(2)
진세노사이드 Rb1은 대표적인 PPD 성분이며 P. notoginseng 에 가장 많이 함유되어 있는 성분이다. Rb1은 인슐린 저항성을 개선하여 항당뇨병제로서 연구되고 있다. Rb1은 인슐린 감수성을 높이고, 에너지 대사와 관련된 AMPK 단백질을 활성화하여 대사조절, 인슐린 신호 전달경로의 부분적 활성화를 통해 포도당 흡수를 촉진한다. 또한, 당지질 대사 조절, B세포의 에이팝토시스를 방지하며, 또한 장내 미생물균총을 조절하여 당뇨병성 합병증을 완화시키는 효능을 가지고 있다고 알려져 있다(6).
2. 진세노사이드 Rb2(3)
진세노사이드 Rb2도 대표적인 PPD 성분이며, 항암, 항염증, 항비만 등에 효과적이다. 특히 고지방식(HFD)을 먹인 마우스 모델에 Rb2를 투여하면 포도당 내성(glucose tolerance)과 인슐린 민감도를 개선하여 체중을 효과적으로 줄이고, 에너지 소비를 유도할 수 있다. 또한, HFD가 지방세포의 크기를 커지게 하지만, Rb2는 효과적으로 크기와 형태를 개선하였다. 비만은 여러 합병증을 유도하여 질병을 초래한다. 진세노사이드 Rb2는 천연물 비만치료에 대한 유의미한 결과를 얻었다(7, 8).
3. 진세노사이드 Rc(5)
진세노사이드 Rc는 PPD형 사포닌 중 하나이며, 항산화, 항암, 항비만, 항염 등에 효과가 있다. TNF-α는 류마티스 관절염을 촉진하는 사이토카인이다. Rc는 TNF-α를 억제함으로 항염작용을 한다는 것이 밝혀졌다. 또한, Rc는 NOX2의 발현을 감소시켜 반응성 산소종(ROS)을 억제하는 항산화 효과도 있다(9).
4. 진세노사이드 Rd(6)
진세노사이드 Rd는 PPD형 사포닌 중 하나이며, 항산화, 항염증, 항세포자멸사, Ca2+ 유입억제 및 미토콘드리아 보호 등을 이용하여 신경보호제로 사용될 수 있다. Ca2+를 차단함으로 허혈성 뇌졸중에 대한 신경보호효과가 입증되었다. 또한 trimethyltin(TMT)은 중추신경계 내 다양한 영향을 미치는 강력한 신경독성 물질로 Rd는 TMT로 인한 발작과 해마 기능장애로 인한 공간학습과 기억력 저하 등을 감소시켰다(10, 11).
5. 진세노사이드 Re(22)
진세노사이드 Re는 PPT형 사포닌 중 하나이며, 항산화, 항염, 항당뇨, 항염 등의 효과가 있다. 6-Hydroxydopamine (6-OHDA)는 뉴런으로 전달되면 쉽게 산화되어 반응성 산소종(ROS)이 형성되는데, 이는 신경독성을 나타낸다. 이때 Re는 GPX4를 조절하며, 산화스트레스를 감소시켜 신경손상을 감소시킨다(12, 13).
6. 진세노사이드 Rf(23)
진세노사이드 Rf는 아시아 인삼에서 미량으로 발견되는 PPT형의 진세노사이드이다. Mouse를 이용한 실험에서 항우울증의 효과를 나타내었다. Mel-Ab 세포에서 티로시나제 발현을 억제하여 멜라닌 생성을 억제하는 기능을 보여주어 천연 미백 제품으로써 연구가 진행되고 있다(14, 15).
7. 진세노사이드 Rg1(24)
진세노사이드 Rg1은 공복 시 고혈당증 발병의 원인이 되는 글루카곤으로 매게 포도당신생성합성을 억제하는 것으로 나타났다. Rg1은 글루카곤에 의해 활성화되는 전사인자 Fox01을 발현을 억제하여 gluconeogenesis의 생성을 억제한다. Rg1은 인슐린 신호전달 경로 조절 외의 당뇨병 치료제로 약리학적 효과가 있음을 보여주었다(16). 또한, 진세노사이드 Rg1은 스트레스로 인한 해마의 손상을 막아 항염증, 항세포자멸사 효과를 보여 우울증치료제의 새로운 가능성을 보여준다(17).
8. Compound K
Compound K는 천연의 인삼에서는 거의 발견되지 않는 주요 진세노사이드로부터 변형된 PPD형 2차 진세노사이드이다. 용해성이 높아 신체에 잘 흡수되어 이용가치가 최근 활발한 연구가 이루어지고 있다. Compound K는 간 항산화, 항염증, 죽상 동맥 경화증 방지, 당뇨병 방지, 항암, 신경 보호 등 다양한 약리학적 효과가 있으며, 히아루론산 생성 증가를 통해 노화 방지 및 피부 보호 효과가 있어 화장품성분으로 활발히 연구가 이루어지고 있다(18). 90% 이상의 진세노사이드는 major 진세노사이드로서 분자량이 큰 배당체 형태여서 생체 내 흡수율이 낮으나, 섭취 시 장내 미생물에 의해 당 가수분해되어 흡수가 용이한 크기의 compound K가 형성된다. 인삼의 Rb1, Rb2 및 Rc 등이 사람의 장내 미생물에 의해 compound K가 생성되는데, 사람의 장내 미생물에 종류와 분포가 달라 인삼을 섭취하여도 사람마다 효능의 차이가 발생한다. 또한, 충치균(Streptococcus mutans) 등을 포함한 포도상구균속(Staphylococcus) 균주, 바실루스 서브틸리스(Bacillis subtilis) 등에 항균 효과가 있음이 보고되어 있다. 그러나 또 다른 연구에 의하면 특이하게 피부상재균인 Candida albicands, Staphylococus aureus, Staphylococus epidermis 등에는 저해효능을 거의 보이지 않으면서 여드름 원인균주에 대해서 선택적 항균효과가 있음을 보여, 향후 여드름 완화용 화장품 개발에 compound K가 매우 우수한 소재가 될 수 있을 것으로 보인다(19-21).
Ⅲ. 결 론
현재 인삼 사포닌 성분들은 다양한 연구분야에서 많은 효능들이 밝혀지고 있다. 암세포 억제작용, 항균효과 등의 의학적 분야와 식품 및 기능성 화장품 원료로써 활용되고 있다. 한국의 인삼은 성분과 특성이 우수하여 나고야의정서 등 국제 자원확보의 시대에 다양하게 활용할 필요가 있으며, 국내에서도 지역에 따른 차이도 있을 수 있어 이에 대한 기본적인 연구도 필요하다. Compound K와 같은 항암, 항균 효능이 뛰어난 소재를 얻기 위한 생산공정으로써 생물전환을 이용하여 대량생산이 가능해지고 있다. 이러한 소재를 이용하여 신제품을 개발하는 것은 인삼의 차별화된 브랜드 개발 및 우리나라만의 고유하고 특화된 제품을 지속적으로 개발하는데 필수 요소라 할 수 있다. 특화된 고유의 원료소재화를 상용화함에 있어 문헌연구 및 소재 확보 등의 기초연구가 더 필요하다. 이를 통해 향후 국제 경쟁력을 가진 사포닌 함유 제품으로 개발하여 고부가가치 창출이 기대된다. 인삼은 한국의 대표 제품군이나, 일부 홍삼제품 이외의 인삼제품은 수년간 판매, 수출이 증가되지 않고 정체되어 있다. 해외 인삼시장 제품은 연 8%대로 급격히 증가하는데, 이에 대한 대책 및 시대에 맞는 새로운 방향 모색이 필요하다. 이러한 문제들을 해결하기 위해서는 인삼에서 얻을 수 있는 사포닌의 새로운 기능성 또는 약리효과를 찾아내는 것이 급선무이다.
사 사
이 논문은 2021년 한국교통대학교의 지원을 받아 수행하였음.
참고문헌
Qi LW, Wang CZ, Yuan, CS. (2011) Isolation and analysis of ginseng: Advances and challenges. Nat Prod Rep. 28, 467~95.

,

,


Shi ZY, Zeng JZ, Wong AST. (2019) Chemical structures and pharmacological profiles of ginseng saponins. Molecules. 24, 2443.

,

,


Lu JM, Yao Q, Chen, C. (2009) Ginseng compounds: An update on their molecular mechanisms and medical applications. Curr Vascul Pharma. 7, 293~302.

,

,


Bai L, Gao J, Wei F, et al. (2018) Therapeutic potential of ginsenosides as an adjuvant treatment for diabetes. Front Pharma. 9, 423.

,

,


Sharma A, Lee, HJ. (2020) Ginsenoside compound K: Insights into recent studies on pharmacokinetics and health-promoting activities. Biomolecules. 10, 1028.

,

,


Zhou P, Xie W, He S, et al. (2019) Ginsenoside Rb
1 as an anti-diabetic agent and its underlying mechanism analysis. Cells. 8, 204.

,

,


Fan W, Huang Y, Zheng H, et al. (2020) Ginsenosides for the treatment of metabolic syndrome and cardiovascular diseases: Pharmacology and mechanisms. Biomed Pharma. 132, 110915.

,


Lin Y, Hu Y, Hu X, et al. (2020) Ginsenoside Rb
2 improves insulin resistance by inhibiting adipocyte pyroptosis. Adipocyte. 9, 302~12.

,

,


Yu T, Yang Y, Kwak YS, et al. (2017) Ginsenoside Rc from
Panax ginseng exerts anti-inflammatory activity by targeting TANK-binding kinase 1/interferon regulatory factor-3 and p38/ATF-2. J Ginseng Res. 41, 127~33.

,

,


Zhang C, Liu X, Xu H, et al. (2020) Protopanaxadiol ginsenoside Rd protects against NMDA receptor-mediated excitotoxicity by attenuating calcineurin-regulated DAPK1 activity. Sci Rep. 10, 1~14.

,

,


Hou J, Xue J, Lee M, Sung C. (2017) Ginsenoside Rd as a potential neuroprotective agent prevents trimethyltin injury. Biomed Rep. 6, 435~40.

,

,


Madhi I, Kim JH, Shin JE, Kim Y. (2021) Ginsenoside Re exhibits neuroprotective effects by inhibiting neuroinflammation via CAMK/MAPK/NF-κB signaling in microglia. Mole Med Rep. 24, 1~10.

,

,


Lee GH, Lee WJ, Hur J, et al. (2020) Ginsenoside Re mitigates 6-hydroxydopamine-induced oxidative stress through upregulation of GPX4. Molecules. 25, 188.

,

,


Kim Y, Lee HY, Choi YJ, Cho SH. (2020) Antidepressant effects of ginsenoside Rf on behavioral change in the glial degeneration model of depression by reversing glial loss. J Ginseng Res. 44, 603~10.

,

,


Lee HR, Jung JM, Seo JY, Chang SE, Song Y. (2021) Anti-melanogenic property of ginsenoside Rf from
Panax ginseng via inhibition of CREB/MITF pathway in melanocytes and
ex vivo human skin. J Ginseng Res. 45, 555~64.

,

,


Liu Q, Zhang FG, Zhang WS, et al. (2017) Ginsenoside Rg1 inhibits glucagon-induced hepatic gluconeogenesis through Akt-FoxO1 interaction. Theranostics. 7, 4001.

,

,


Li Y, Wang L, Wang P, et al. (2020) Ginsenoside-Rg
1 rescues stress-induced depression-like behaviors via suppression of oxidative stress and neural inflammation in rats. Oxid Med Cell Longev. 2020, article ID 2325391.

,

,


Sharma A, Lee HJ. (2020) Ginsenoside compound K: Insights into recent studies on pharmacokinetics and health-promoting activities. Biomolecules. 10, 1028.

,

,


Kim M, Kim JI, Jung KH, et al. (2021) Biosynthesis of compound K, a biologically active saponin of ginseng (
Panax ginseng) by bioconversion. J Kor Appl Sci Tech. 38, 1335~44.

Kim M, Shin HY, Kim HG, et al. (2021) Anti-inflammatory activity and toxicity of the compound K produced by bioconversion. J Kor Appl Sci Tech. 38, 1467~76.

Jegal J, Jeong EJ, Yang MH. (2019) A review of the different methods applied in ginsenoside extraction from
Panax ginseng and
Panax quinquefolius roots. Nat Prod Comm. 14, 1~10.